* Your assessment is very important for improving the workof artificial intelligence, which forms the content of this project
Download A táplálékfelvétel, a só- és vízháztartás neuroanatómiája
Haemodynamic response wikipedia , lookup
Neuroplasticity wikipedia , lookup
Feature detection (nervous system) wikipedia , lookup
Activity-dependent plasticity wikipedia , lookup
NMDA receptor wikipedia , lookup
Nervous system network models wikipedia , lookup
Premovement neuronal activity wikipedia , lookup
Axon guidance wikipedia , lookup
Central pattern generator wikipedia , lookup
Synaptogenesis wikipedia , lookup
Neuroanatomy wikipedia , lookup
Aging brain wikipedia , lookup
Metastability in the brain wikipedia , lookup
Channelrhodopsin wikipedia , lookup
Signal transduction wikipedia , lookup
Pre-Bötzinger complex wikipedia , lookup
Optogenetics wikipedia , lookup
Sexually dimorphic nucleus wikipedia , lookup
Stimulus (physiology) wikipedia , lookup
Molecular neuroscience wikipedia , lookup
Synaptic gating wikipedia , lookup
Circumventricular organs wikipedia , lookup
Clinical neurochemistry wikipedia , lookup
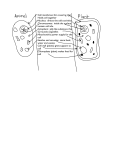
Funkcionális neuroanatómia 5. A táplálékfelvétel, a só- és vízháztartás neuroanatómiája 2011 - Neuromorfológia PhD program food intake receptors gastrointestinal brain food intake receptors gastrointestinal brain humoral inputs NTS / AP hypothalamic CIRCUMVENTRICULAR ORGANS subfornical organ area postrema OVLT arcuate nucleus subcommissural organ Circumventricularis szervek Kamrakörüli területek gazdag vérellátással, ahol hiányzik a vér-agy gát. Az állatvilágban, főleg a phylogenesis alsóbb fokán igen jelentősek, emberben nem mindegyik található meg. Ide soroljuk a szubfornikális szervet, az area postremát, az eminentia medianát a nucleus arcuatus egy részével, és az organum vasculosum laminae terminalist. Tágabb értelemben ide tartozik a hypophysis hátsó lebenye és a corpus pineale is. Area postrema Az ún. circumventriculáris szervek közé tartozik, melyek az agykamrák falánál jellegzetes sejtcsoportokat alkotnak, területükön nincs vér-agy gát. Mint ilyen, az area postrema, mely emberben az obexnél a IV. kamra két oldalán helyezkedik el, a nyúltvelő „nyitott kapujának” tekinthető, melynek erein át a nyúltvelő viszceroszenzoros központja (nucleus tractus solitarii) humorális afferentációt kap. Az area postremát a n. vagus idegzi be. Sokáig „hányás központ”-ként volt ismeretes. AP Szubfornikális szerv – SFO (subfornical organ) Vér-agy gát-mentes circumventriculáris szerv, a hypothalamus egyik „kapuja”, a foramen interventricularénál domborodik be a kamraüregbe. Az agy angiotensin II. receptorban leggazdagabb területe. Rostjai a lamina terminalis mentén érik el a preopticus areát és az elülső hypothalamust. vHC LV vHC vHC LV III. III. LV rat human 3V LEPTIN - acts on the brain to inhibit feeding - the effects of leptin on appetite and energy balance are mediated by hypothalamic neurons: basal hypothalamic lesions prevent leptin action in the brain - brain microvessels bind and internalize leptin. Leptin may gain access to neurons by receptor mediated transcytosis - leptin receptors (Ob-Rb) are expressed by arcuate, paraventricular, ventromedial and dorsomedial neurons - leptin reduces NPY levels and NPY mRNA expression in the arcuate nucleus - leptin stimulates POMC mRNA expression in the arcuate, CRH mRNA expression in the paraventricular nucleus - leptin activates CART neurons in the arcuate nucleus that project to sympathetic preganglionic neurons in the spinal cord INSULIN - insulin stimulates leptin expression and release - insulin activates sympathetic activity and thermogenesis - insulin receptors and insulin receptor substrate protein (IRS-1) are expressed in arcuate neurons - insulin inhibits NPY expression in the arcuate nucleus GHRELIN - ghrelin stimulates food intake - it is predominantly synthesized in the stomach - it stimulates NPY, CRH and growth hormone release - it is also expressed in the arcuate nucleus - NPY appears to be important in mediating the orexigenic action of ghrelin food intake receptors gastrointestinal brain humoral inputs NTS / AP hypothalamic neuronal pathways vagal afferents NEURONAL INPUTS - to the NTS - vagal inputs (from the stomach and the duodenum) - taste signals (facial and glossopharyngial) Nucleus tractus solitarii (Nucleus of the solitary tract – NTS) Primer viszceroszenzoros mag a nyúltagy dorsalis részében. Viszceroszenzoros általános és viszceroszenzoros speciális (ízérző) rostok kapcsolódnak itt át. Rostokat kap a gerincvelőből is (tractus spinosolitarius). Felszálló viszceroszenzoros rostjai az amygdalában és a hypothalamusban, ízérző rostjai az insuláris kéregben végződnek. Az NTS érző neuronjai a vagus viszceromotoros neuronjaival (nucleus motorius dorsalis vagi) az autonóm szabályozó reflexívek részei. Artériás ellátása egyedi a dorsális medullában, a posterior inferior cerebelláris artéria látja el az area postremán keresztül. Az erek jelentős részén nincs vér-agy gát, így az NTS a nervus vaguson és a gerincvelőn kívül jelentős humorális afferentációt is kap. NUCLEUS OF THE SOLITARY TRACT - gastrointestinal viscerosensory nerve terminals - glucagon-like peptide-1, CCK, NPY, somatostatin - CCKA receptors - leptin, ghrelin and insulin receptors - m, d, k opiate receptors - CB1 receptors - m-opiate receptor agonist injected into the NTS stimulates food intake - short-term signals related to the quality and quantity of food ingested food intake receptors gastrointestinal brain humoral inputs NTS / AP hypothalamic neuronal pathways vagal afferents NTS – ascending food intake NEURONAL INPUTS - short-term signals related to the quality and quantity of food ingested - strech- and mechanoreceptors trigger signals to the CNS through vagal nerve - signals are relayed in the nucleus of the solitary tract (NTS) and ascending fibers terminate in the paraventricular, ventromedial and dorsomedial hypothalamic nuclei food intake NEURONAL INPUTS - short-term signals related to the quality and quantity of food ingested - strech- and mechanoreceptors trigger signals to the CNS through vagal nerve - signals are relayed in the nucleus of the solitary tract (NTS) and ascending fibers terminate in the paraventricular, ventromedial and dorsomedial hypothalamic nuclei Nucleus paraventricularis hypothalami A hypothalamus egyik legjelentősebb magja, magno- és parvocellularis részre osztható. A magnocelluláris neuroszekretoros sejtek vasopressint és oxytocint termelnek, axonjaik a tractus hypothalamo-hypophysealis egy részét alkotják, és a hypothalamus hátulsó lebenyében végződnek. A parvocelluláris neuroszekretoros idegsejtek több peptiderg neurohormont (corticotropin-releasing hormon – CRH, thyrotropin-releasing hormon – TRH, vasopressin) és neuromodulátort (neuropeptidet) termelnek. A parvocellularis neuronok egy része az eminentia mediana portális erei révén juttatja el termékét a hypophysis elülső lebenyébe, másik részük a nyúltvelőbe és a gerincvelőbe projíciál. A CRH-termelő idegsejtek révén a paraventriculáris magot a stresszválasz központi részének, a „hypothalamohypophysis-mellékvesekéreg szabályozó rendszer” („HPA axis”) kiinduló pontjának tekintik. Nucleus arcuatus A hypothalamus magja a III. kamra alsó részének két oldalán, a retrochiasmaticus area és a corpus mamillare kezdete között, közvetlenül az eminentia medianától dorsolaterálisan. Sejtjeik számos neuropeptidet és peptid receptort, egy részük dopamint (A12 catecholamin sejtcsoport) termel. Emberben nucleus infundibularisnak is nevezik. Neuronjai a hypothalamus más magjaihoz és a nyúltvelői és gerincvelői autonóm sejtekhez projíciálnak. A mag mediális részében nincs vér-agy gát. Jelentős szerepet visz a táplálékfelvétel idegrendszeri szabályozásában. Nucleus dorsomedialis hypothalami A hypothalamus középső részében, a harmadik agykamra két oldalán, a nucleus ventromedialis felett helyezkedik el. Neuronjai több szubdivíziót alkotnak, melyek a táplálékfelvétel központi szabályozásában és a stressz válaszban visznek szerepet. VENTROMEDIAL NUCLEUS - lesioning of this nucleus (electrolytic or gold thioglucose) induces hyperphagia and resulted in extreme obesity - stimulation of ventromedial neurons suppress feeding - injections of leptin and urocortin into the nucleus inhibit, injections of NPY, β-endorphin or galanin stimulate feeding - local administration of 2-deoxy-glucose (cellular glucoprivation) evokes rapid increases in plasma levels of glucose food intake receptors gastrointestinal brain humoral inputs NTS / AP hypothalamic neuronal pathways vagal afferents NTS – ascending hypothalamic circuits INTRAHYPOTHALAMIC NEURONAL CIRCUITS - arcuate – PVN projection - arcuate – dorsolateral hypothalamic projections - intraarcuate interactions - intrahypothalamic orexin projections NEUROPEPTIDE Y (NPY) - NPY is the most potent orexigenic agent known - NPY neurons in the arcuate nucleus co-express AgRP - arcuate preproNPY mRNA level is increased by food deprivation - arcuate NPY cells express leptin receptors (Ob-Rb form) - expression of NPY mRNA in the arcuate nucleus is inhibited by leptin and insulin - the appetite-promoting effect of NPY is mediated by NPY Y5 receptors - glucose, as well as carbohydrate-reach meal causes rapid increase in NPY level and NPY mRNA expression in the arcuate nucleus - 2-deoxy-glucose, which blocks glucose utilization stimulates the expression and production of NPY in the arcuate nucleus AGOUTI-RELATED PEPTIDE (AgRP) - AgRP-NPY neurons in the arcuate nucleus project to the paraventricular and dorsomedial nuclei, act on MCR4 receptors to increase feeding - AgRP injections into the paraventricular nucleus result in a long-lasting food intake - leptin inhibits AgRP expression in arcuate neurons - AgRP blocks the inhibitory action of POMC on food intake - AgRP binds to MC4 receptors and antagonize the action of α-MSH PRO-OPIOMELANOCORTINS (POMC) - leptin stimulates POMC expression in the arcuate nucleus - POMC and leptin receptors are co-expressed in arcuate neurons - POMC is co-expressed with CART peptide - α-MSH released from arcuate POMC axons in the paraventricular nucleus exerts anorexic effects by acting on MC4 receptors CART (cocaine- and amphetamine-regulated trascript) PEPTIDE - CART mRNA expression is down-regulated in food-deprived rats - I.c.v. given CART inhibits food intake - CART peptide blocks the feeding response induced by NPY - CART cells in the arcuate nucleus express leptin receptors - CART expression in the arcuate nucleus is stimulated by leptin OREXINS (HYPOCRETINS) - orexin enhances food intake when injected into the hypothalamus - orexin levels are markedly elevated during starvation and decrease by refeeding - food deprivation (48 h) upregulates prepro-orexin mRNA levels in the hypothalamus - orexin expression is blocked by leptin - orexin cells are innervated by arcuate NPY and POMC fibers - orexin-1 receptors are present in the ventromedial, orexin-2 receptors in the paraventricular nucleus MELANIN CONCENTRATING HORMONE (MCH) - MCH has a stimulatory effect on feeding: i.c.v. given MCH increases food intake - MCH expression is inhibited by leptin - MCH neurons co-express leptin receptors - there are abundant NPY terminals of arcuate origin on MCH neurons GALANIN - endogenous galanin contributes to the natural appetite for fat - central administration of galanin produces a strong feeding response - leptin and insulin inhibit galanin mRNA expression - galanin is present in the paraventricular and arcuate nuclei and in the lateral hypothalamus CART (cocaine- and amphetamine-regulated trascript) PEPTIDE - CART mRNA expression is down-regulated in fooddeprived rats - I.c.v. given CART inhibits food intake - CART peptide blocks the feeding response induced by NPY - CART cells in the arcuate nucleus express leptin receptors - CART expression in the arcuate nucleus is stimulated by leptin UROCORTINS - urocortin III. neurons are located in the dorsomedial hypothalamus with ventromedial projections - urocortin III. neurons here co-express enkephalin - neurons here contain leptin receptors (Ob-Rb receptors) - neurons here are activated by leptin (c-fos expression) - urocortin III. acts on CRH2 receptors in the ventromedial nucleus - urocortin acts as endogenous activators of anorexia. Its anorexic effect appears to be more potent than that of CRH PARAVENTRICULAR NUCLEUS - lesioning of the nucleus induces hyperphagia - hypoglycemia increases c-fos and CRH mRNA expressions in the nucleus - paraventricular CRH increases sympathetic output and results in a long-lasting reduction of food intake (anorexic effect) - leptin activates neurons innervating the paraventricular nucleus - CRH2 receptors mediate the inhibitory effect on feeding STIMULATION OF FOOD INTAKE INHIBITION OF FOOD INTAKE OREXIGENIC PEPTIDES ANOREXIGENIC PEPTIDES neuropeptide Y (NPY) agouti-related peptide (AgRP) orexins (hypocretins) melanin concentrating hormone (MCH) galanin β-endorphin dynorphins ENDOCANNABINOIDS POMC (especially a-MSH) CART peptide corticotropin releasing hormone (CRH) urocortin III cholecystokinin (CCK) glucagon-like peptide (GLP-1) PrRP CGRP amylin ENDOCANNABINOIDS - both peripheral and central administrations of anandamide stimulate food intake - anandamide and 2-arachidonoyl-glycerol (2-AG) levels in the hypothalamus are reduced by leptin - CB1 receptor antagonist, SR141716 suppresses appetite, reduces food intake and body weight - endogenous cannabinoid system may modulate the appetitive value of the food by affecting the activity of brain reward systems - high concentration of CB1 mRNA in the hypothalamic ventromedial nucleus - 2-AG is present in hypothalamic areas involved in feeding - CB1 receptor KO mice eat less and loose body weight - CB1 receptor KO mice show increased CRH mRNA in the paraventricular nucleus and reduced CART mRNA levels in the dorsolateral hypothalamus ANANDAMIDE 1h post mortem INTRAHYPOTHALAMIC NEURONAL CIRCUITS - arcuate – PVN projection - arcuate – dorsolateral hypothalamic projections - intraarcuate interactions - intrahypothalamic orexin projections food intake receptors gastrointestinal brain humoral inputs NTS / AP hypothalamic neuronal pathways vagal afferents NTS – ascending hypothalamic circuits neuronal outputs A SÓ- ÉS VÍZHÁZTARTÁS KÖZPONTI SZABÁLYOZÁSA CRH LH-RH SOM GH-RH Gömöri’s staining Hypothalamo-hypophysis rendszer Két részből, a nagysejtes hypothalamo-neurohypophysealis és a kissejtes tubero-infundibuláris rendszerből tevődik össze. A nagysejtes supraopticus és paraventriculáris neuronok vasopressint és oxytocint termelnek, axonjaik jelentős része (a supraopticus esetében az összes) a neurohypophysisben végződnek, ami quasi raktára a vasopressinnek és az oxytocinnak. A tubero-infundibuláris neuronok a hypophysis elülső részében levő endokrin sejtek neurohormonjaik termelésének szabályozását és felszabadításukat (release-t) végzik. A hypothalamus különböző részeiben termelődő neurohormonok nem közvetlen úton, hanem neurohumorális transzport révén jutnak a hypophysisbe: axonjaik az eminentia mediana vér-agy gátmentes kapillárisaiba ürítik szállított termékeiket, melyek a portális erek révén jutnak a hypophysis elülső lebenyébe. Hypothalamus szerepe a só- és vízháztartás szabályozásában A vasopressin a magnocellularis paraventricularis és supraopticus magokban termelődik. A vasopressint korábban antidiureticus hormonként (ADH) írták le, és ez az elnevezés ma is használatos a klinikumban. A vasopressin szintézisében és a neurohypophysisbe juttatásában, illetve az onnan történő felszabadításában két másik hormon az angiotensin II, és atrialis natriureticus hormon visz szerepet. Az előző a vesében termelődő renin-angiotensin rendszer aktív tagja, mely a vér-agy-gát-mentes subfornicalis szerven keresztül jut be az agyba, míg az utóbbit a preopticus area neuronjai termelik. Nucleus tractus solitarii (Nucleus of the solitary tract – NTS) Primer viszceroszenzoros mag a nyúltagy dorsalis részében. Viszceroszenzoros általános és viszceroszenzoros speciális (ízérző) rostok kapcsolódnak itt át. Rostokat kap a gerincvelőből is (tractus spinosolitarius). Felszálló viszceroszenzoros rostjai az amygdalában és a hypothalamusban, ízérző rostjai az insuláris kéregben végződnek. Az NTS érző neuronjai a vagus viszceromotoros neuronjaival (nucleus motorius dorsalis vagi) az autonóm szabályozó reflexívek részei. Artériás ellátása egyedi a dorsális medullában, a posterior inferior cerebelláris artéria látja el az area postremán keresztül. Az erek jelentős részén nincs vér-agy gát, így az NTS a nervus vaguson és a gerincvelőn kívül jelentős humorális afferentációt is kap. Nucleus paraventricularis hypothalami A hypothalamus egyik legjelentősebb magja, magno- és parvocellularis részre osztható. A magnocelluláris neuroszekretoros sejtek vasopressint és oxytocint termelnek, axonjaik a tractus hypothalamo-hypophysealis egy részét alkotják, és a hypothalamus hátulsó lebenyében végződnek. A parvocelluláris neuroszekretoros idegsejtek több peptiderg neurohormont (corticotropin-releasing hormon – CRH, thyrotropin-releasing hormon – TRH, vasopressin) és neuromodulátort (neuropeptidet) termelnek. A parvocellularis neuronok egy része az eminentia mediana portális erei révén juttatja el termékét a hypophysis elülső lebenyébe, másik részük a nyúltvelőbe és a gerincvelőbe projíciál. A CRH-termelő idegsejtek révén a paraventriculáris magot a stresszválasz központi részének, a „hypothalamohypophysis-mellékvesekéreg szabályozó rendszer” („HPA axis”) kiinduló pontjának tekintik. NUCLEUS ACCUMBENS - the nucleus accumbens has been shown to be particularly involved in mediating the affective response to food - lesions of the accumbens nucleus do not reduce food intake, it might be involved in the rewarding aspects of feeding - feeding responses can be elicited following direct administration of opiates, m- and d-selective opioid receptor agonists into the shell portion of the nucleus - microinjections of GABAA agonist muscimol into the accumbens nucleus exhibit feeding response, activate hypothalamic orexin neurons and inhibit POMC neurons - the nucleus contains high levels of MCH and cannabinoid receptor mRNA Vasopressin